√Hukum Boyle
Namanya juga mencari informasi, tentu dibutuhkan keterbukaan dari Anda, dalam artian bahwa apa yang akan kami jelaskan disini tentu membutuhkan sedikit waktu dalam membacanya baru bisa memahaminya. Untuk itu buka lebar-lebar pikiran Anda supaya dapat menangkap "pengetahuan" baru yang akan kami bahas sebentar lagi. Berikut penjelasannya.
Pembahasan Lengkap Hukum Boyle
Pengertian Hukum Boyle Adalah – Hay sahabat sekalian.!Pada perjumpaan kali ini kembali akan quipper.co.id sampaikan materi tentang makalah Hukum Boyle Namun diperjumpaan sebelumnya, yang mana quipper juga telah menyampaikan materi tentang Kapilaritas. Nah untuk melengkapi apa yang menjadi tema pembahasan kita kali ini maka, simak ulasan selengkap berikut ini.
Pengertian Hukum Boyle

Apa yang dimaksud dengan Hukum boyle yakni merupakan sebuah hukum fisika yang menerangkan mengenai bagaimana adanya suatu hubungan antara tekanan dengan volume pada suatu gas.
Dimana pada mulanya hukum pertama kali ditemukan oleh salah seorang yang bernama Robet Boyle sekitar pada tahun (1627 sampai 1691).
Yang mana pada saat itu Robert melakukan suatu penelitian guna mencari tahu mengenai hubungan antara tekanan dengan volume gas pada suhu yang konstan.
Kemudian dari hasil penelitiannya tersebut, Robet Boyle memperoleh jawaban atas peneliiannya yang mana bahwa hasil kali tekanan dan volume gas yang ada didalam ruangan tertutup ia akan tetap atau konstan.
Dengan adanya pernyataan yangs sesuai dengan hasil penenmuannya maka humuk Robert Boyle ini disesbut dengan Hukum Boyle, yang memiliki bunyi:
“Pada suhu tetap, Adanya tekanan gas yang terjadi didalam suatu ruang tertutup akan berbanding terbalik dengan volumenya”
Rumus Hukum Boyle
Berdasarkan penjelasan diatas yang mana pada pernyataan tersebut diungkapkan mengenai hasil dari hukum boyl tersebut mempunyai makna yakni mengenai hasil dari kali tekanan dan juga volume gas yang berlangsung didalam suatu ruangan yang seluruh bagiannya tidak memiliki celah/ditutup rapat merupakan konstan (tetap) namun syaratnya suhu gas harus dalam keadaan tetap.
Berdasarkan Pernyataan diatas jadi apabila dituliskan ke dalam rumus, ialah:
P.V = C
Diman mana C ialah merupakan suatu bilangan bersifat tetap (konstanta). Apabila tekanan diubah maka volume pada gas tersebut akan berubah juga, jadi rumus diatas bisa ditulis seperti berikut:
P1 . V1 = P2 . V2
Keterangan :
P1 = Merupakan suatu tekanan gas mula-mula (atm.cm Hg, N/m2, Pa)
P2 = Merupakan suatu tekanan gas akhir (atm, cm Hg, N/m2, Pa)
V1 = Merupakan suatu volum gas mula-mula (m3, cm3)
V2 = Merupakan volum gas akhir (m3, cm3)
Namun perlu kalian ketahui bahwa Hukum boylee hanya dapat berlaku dalam keadaan:
- Suhu gas dalam kondisi tetap atau konstan
- Gas harus terdapat didalam sebuah ruangan yang tertutup
- Tidak mengandung suatu reaksi kimia
- Tidak terjadinya suatu perubahan wujud gas
Grafik Hukum Boyle
Apabila digambarkan ke dalam sebuah grafik, maka hukumini akan membentuk menjadi sebuah kurva isoternal. Nah di bawah berupa Grafik Kurva isoternal.
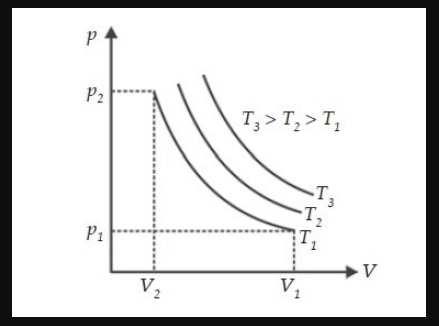
Penerapan Hukum Boyle
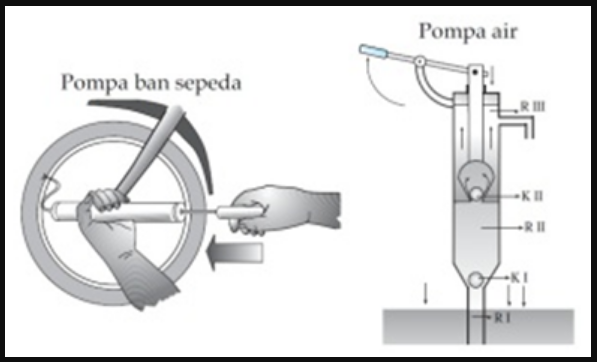
Kemudian menyinggung mengenai penerapan hukum boylle terdapat pada prinsip kerja pompa.
Dimana pompa ialah merupakan sebuah alat yang biasa digunakan untuk memindahkan gas/zat cair. Berdasarkan prinsip kerja ini, maka pompa dapat dikelompokkan atas dua yakni pompa hisap dan pompa tekan.
Pada saat penghisap ditarik, maka volume udara yang terdapat di dalam pompa tersebut akan semakin meningkat/membesar dan udara tidak bisa masuk ke dalam ban sebab harus masuk melalui katup (ventil) dari karet.
Apabila pengisap ditekan maka volume udara didalam sebuah pompa akan menjadi mengecil dan udara bisa masuk ke dalam ban dengan melalui ventil sebab tekanannya akan membesar.
Kemudian Alat sejenis yang menggunakn prinsip hukum boylee ialah seperti misalnya alat suntik, pipet, pompa tekan dan juga pompa hisap.
Contoh Soal Hukum Boyle Dan Pembahasan
Nah berikut terdapat contoh soal dari hukum boylee ang dianatranya ialah sebagai berikut:
Contoh Soal. 1| Di dalam suatu ruangan yang tertutup dimana di dalamnya terdapat unsur gas dengan volume 200 ml. Kemudian apabila tekanan ruangan tersebut ialah 60cmHg, maka berpakah tekanan gas yang ada pada ruangan jika volumenya 150 ml? Pebahasan: Diketahui: V1 = 200 ml P1 = 60 cmHg V2 = 150 ml Jika Ditanya: P2…? Jawaban: Jadi tekanan gas yang ada pada ruangan jika volumenya 150 ml menurut hukum boyle ialah sebesar 80 cmHg. |
Contoh Soal. 2| Pada sebuah ruang yang seluruhnya tertutup dengan memiliki volume 0,2 m3 kemudian berisi gas dengan tekanan sebesar 60.000 Pa. Maka hitunglah berapa jumlah volume gas jika pada tekanan ditingkatkan menjadi 80.000 Pa? Pembahasan: Diketahui: P1 = 60.000 Pa V1 = 0.2 m3 P2 = 80.000 Pa Ditanya: V2…? Jawab: P1 V1 = P2 V2 V2 = (P1 V1) : P2 V2 = (60.000 x 0,2) : 80.000 V2 = 1,2/8 V2 = 0,15 m3 Maka, volume pada gas tersebut akan menjadi 0,15 M3 |
Nah itulah yang bisa quipper.co.id sampaikan mengenai Hukum Boyle, semoga apa yang telah disampaiakan kali ini dapat bermanfaat bagi sahabat semua. Baca Juga : Konduktor dan Isolator
The post Hukum Boyle appeared first on Quipper.Co.Id.
Itulah tadi ulasan tentang Hukum Boyle yang dapat kami sampaikan untuk Sobat pembaca semuanya. Tak lupa kami ucapkan banyak terima kasih karena sudah mengunjungi situs quippercoid. blogspot. com dan membaca urian diatas hingga selesai. Semoga apa yang kami sampaikan diatas dapat menambah wawasan kita semuanya, tertama untuk Anda yang memang sedang mencarinya. Ingat untuk selalu bahagia dan sampai jumpa di postingan selanjutnya.
Post a Comment for "√Hukum Boyle"